Bases de datos genómicos y su apoyo a la farmacogenómica
En la última década, el advenimiento de la genómica ha revolucionado el campo de la medicina moderna. Las bases de datos genómicos han surgido como herramientas clave que permiten una comprensión más profunda de la diversidad genética humana y cómo esta diversidad influye en la respuesta a los medicamentos. Este avance no solo promueve un enfoque personalizado en el tratamiento de las enfermedades, sino que también permite la identificación de subgrupos de pacientes que pueden beneficiarse de terapias específicas. En este contexto, la farmacogenómica se presenta como el puente que conecta la información genética con la práctica clínica, mejorando así la eficacia de los tratamientos médicos y minimizando riesgos adversos.
Este artículo explora la intersección entre las bases de datos genómicos y la farmacogenómica, resaltando cómo el acceso a información genética de alta calidad ha facilitado un enfoque más estratégico en el desarrollo y la administración de medicamentos. A lo largo de este texto, se analizarán diversos aspectos relevantes, desde la infraestructura de las bases de datos genéticas hasta las implicaciones éticas que surgen en esta era de la medicina personalizada, con el fin de proporcionar una visión integral del estado actual y futuro de estas tecnologías en la salud.
- La importancia de las bases de datos genómicos
- Farmacogenómica: el vínculo entre genética y medicamentos
- Desarrollo de bases de datos genómicos
- Implicaciones del uso de bases de datos genómicos para la farmacogenómica
- Retos y consideraciones éticas
- Conclusiones sobre bases de datos genómicos y farmacogenómica
La importancia de las bases de datos genómicos
Las bases de datos genómicos son repositorios que contienen información genética de individuos y poblaciones. Su función principal es almacenar y proporcionar acceso a datos que pueden ser utilizados por investigadores y médicos para entender variaciones genéticas y su relación con diversas condiciones de salud. Entre las bases más reconocidas se encuentran el Proyecto del Genoma Humano, que mapeó la secuencia completa del ADN humano, y bases de datos específicas como ClinVar, que brinda información sobre la relación entre variantes genéticas y resultados clínicos.
La ampliación del acceso a las bases de datos genómicos ha sido fundamental para la investigación en farmacogenómica. Estos recursos permiten la integración de datos genéticos con información sobre medicamentos y su interacción con variaciones genéticas específicas. A través de esta integración, los científicos pueden identificar patrones que ayuden a predecir cómo responderán diferentes personas a tratamientos farmacológicos. Esta capacidad no solo mejora la eficacia de los tratamientos, sino que también ayuda a reducir los efectos secundarios, permitiendo una medicina más segura y efectiva.
Farmacogenómica: el vínculo entre genética y medicamentos
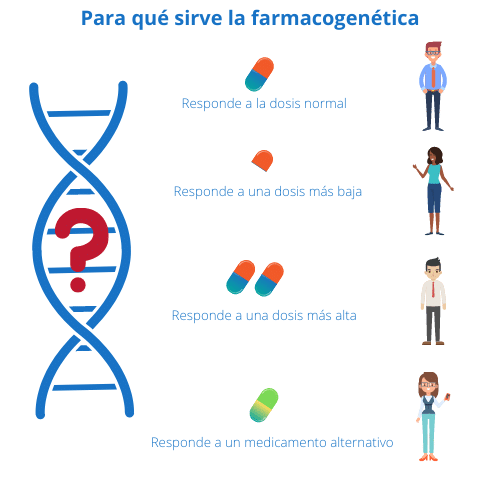
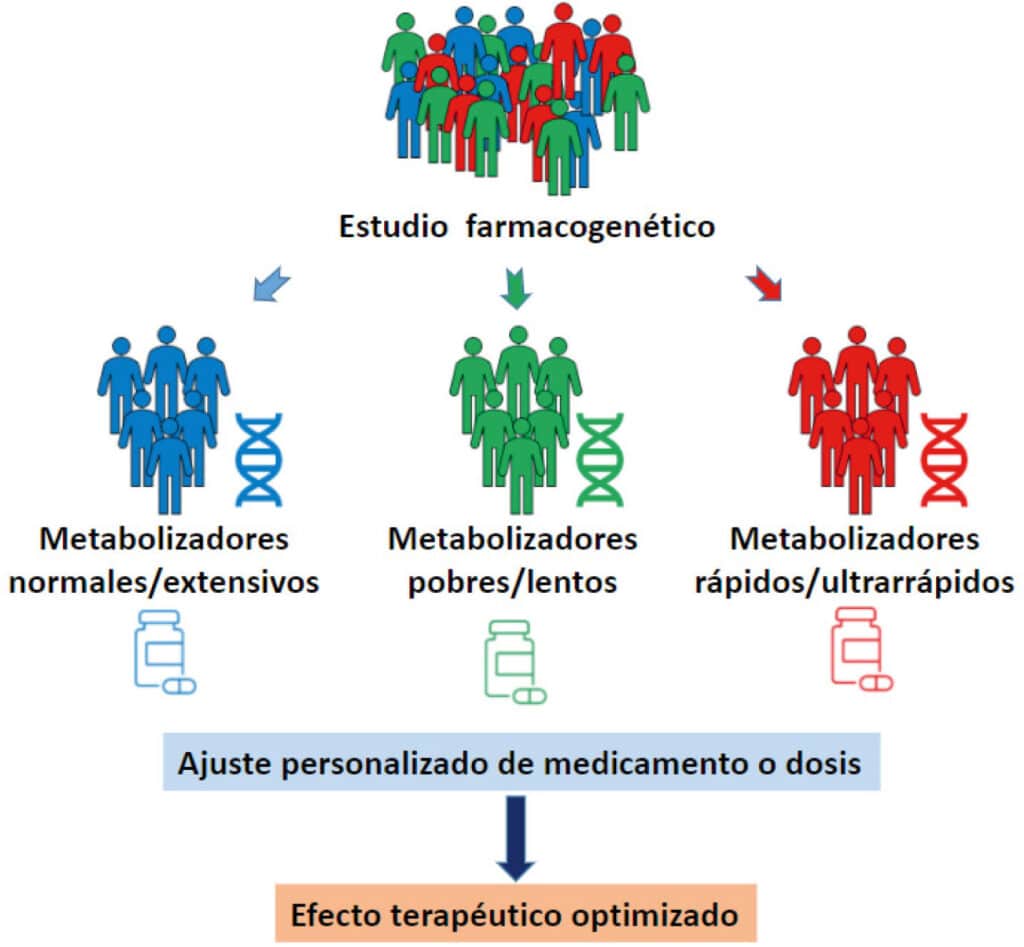
La farmacogenómica se refiere al estudio de cómo los genes afectan la respuesta de los organismos a los medicamentos. Este campo considera las variaciones en el ADN que pueden influir en la eficacia y seguridad de los tratamientos, llevando a la personalización de la medicina. La integración de datos de bases genómicas y farmacogenómicas permite la creación de perfiles genéticos individuales y orienta a los médicos en la selección del tratamiento más adecuado para cada paciente.
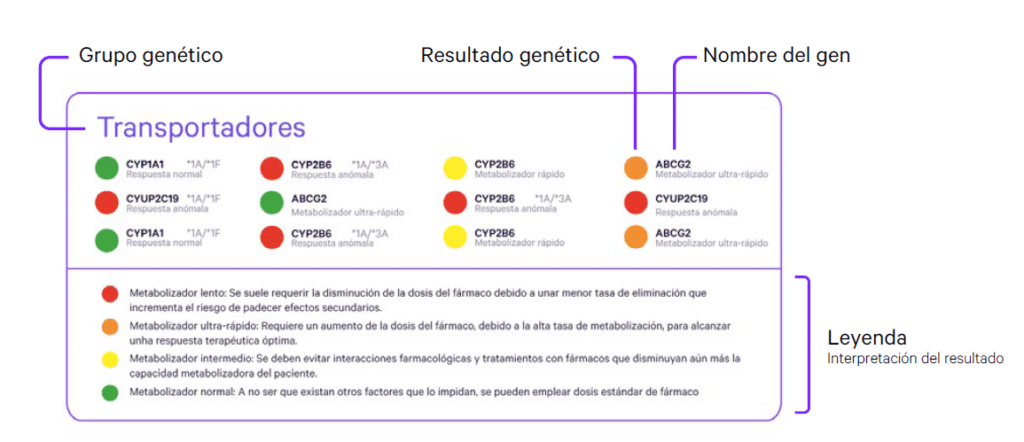
Por ejemplo, la variación en el gen CYP450 puede influir en cómo metabolizamos determinados medicamentos. Algunas personas pueden tener versiones del gen que les make metabolizar rápidamente, mientras que otras pueden hacerlo de manera más lenta. Esto puede resultar en dosis ineficaces o efectos adversos graves. Al consultar las bases de datos genómicos, los médicos pueden ajustar las dosis de medicamento y, a su vez, mejorar los resultados clínicos.
Desarrollo de bases de datos genómicos
El desarrollo de bases de datos genómicos ha estado guiado por la rápida evolución de la tecnología de secuenciación del ADN. Las técnicas de secuenciación de alto rendimiento han permitido la creación de enormes volúmenes de datos genéticos en un período de tiempo relativamente corto. Esto ha abierto la puerta a una mayor comprensión de la diversidad genética dentro de diferentes poblaciones y cómo esta diversidad afecta la salud.
Además, hay un esfuerzo continuo por mejorar la calidad de los datos disponibles. La normalización y la estandarización de los datos genómicos son cruciales para asegurar que los análisis realizados sean comparables y replicables. Las bases de datos deben actualizarse regularmente a medida que se obtienen nuevos descubrimientos y se validan nuevas variantes genéticas, lo que requiere una infraestructura robusta y recursos financieros significativos.
Implicaciones del uso de bases de datos genómicos para la farmacogenómica
El uso de bases de datos genómicos en el contexto de la farmacogenómica presenta implicaciones significativas tanto para la investigación como para la práctica clínica. A nivel de investigación, estas bases de datos permiten la identificación de biomarcadores genéticos que pueden ser utilizados para predecir la respuesta a tratamientos específicos. Esto no solo acelera el desarrollo de nuevos fármacos sino que también optimiza el proceso de aprobación de medicamentos por parte de agencias regulatorias.
A nivel clínico, la implementación de recomendaciones basadas en farmacogenómica puede ser un desafío. Los médicos deben estar capacitados para interpretar los datos genómicos y aplicar esa información en la toma de decisiones clínicas. La falta de integración de la farmacogenómica en la práctica estándar variará dependiendo de la región geográfica y de los sistemas de salud. Es fundamental abordar estos desafíos para garantizar que los beneficios de la farmacogenómica se traduzcan en mejores resultados de salud para los pacientes.
Retos y consideraciones éticas
La utilización de bases de datos genómicos en la farmacogenómica también plantea retos y consideraciones éticas importantes. Uno de los principales problemas es la privacidad de los datos genéticos. A medida que se recopila y almacena más información genética, surge la pregunta de cómo se protegerán estos datos de posibles usos indebidos. Las políticas y normas de ética deben evolucionar para asegurar que la información genética de los pacientes se maneje de manera responsable y que los pacientes estén debidamente informados sobre el uso de sus datos.
Además, existe la preocupación sobre el potencial de sesgos en los datos genómicos que podrían afectar la equidad en el acceso a tratamientos personalizados. La representación insuficiente de grupos minoritarios en las bases de datos genómicos puede llevar a que los medicamentos no se desarrollen ni se ajusten adecuadamente para todos los grupos de población. Esto requiere un esfuerzo consciente por parte de la comunidad científica y médica para asegurar que los estudios sean inclusivos y representativos.
Conclusiones sobre bases de datos genómicos y farmacogenómica
Las bases de datos genómicos juegan un papel fundamental en la avanzadilla de la farmacogenómica, proporcionando la información necesaria para hacer tratamientos más precisos y eficaces. Los beneficios de vincular datos genéticos con información sobre medicamentos son innumerables, al igual que las oportunidades para mejorar la atención médica a través de la medicina personalizada. Sin embargo, es crucial abordar los desafíos asociados con la privacidad de los datos, la calidad de la representación en las bases de datos y las consideraciones éticas alrededor de su uso.
El futuro de la farmacogenómica dependerá de una colaboración continua entre investigadores, médicos y responsables políticos para optimizar el uso de bases de datos genómicos. Solo así se podrá garantizar un acceso equitativo y seguro a los tratamientos farmacológicos adaptados a las necesidades de cada individuo, mejorando así la calidad y efectividad de los cuidados de salud en todo el mundo.
Si quieres conocer otros artículos parecidos a Bases de datos genómicos y su apoyo a la farmacogenómica puedes visitar la categoría Farmacogenómica.




Deja una respuesta