Bioinformática: Aplicaciones en la investigación del cáncer
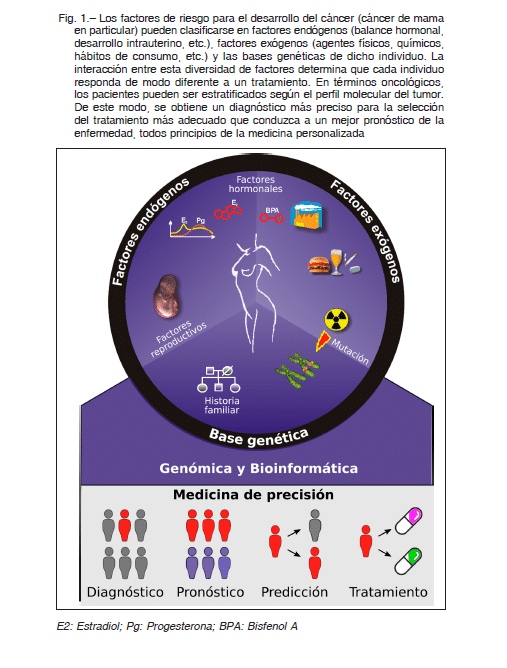
La bioinformática ha emergido como una disciplina crucial en la biología moderna, especialmente en el área del estudio del cáncer. Con el avance de las tecnologías de secuenciación y el crecimiento exponencial de datos biológicos, los investigadores de cáncer están equipados más que nunca para desentrañar los complejos mecanismos biológicos encargados del desarrollo tumoral. Este campo multidisciplinario fusiona la biología, la informática y la estadística para analizar, interpretar y visualizar datos biológicos, lo que resulta fundamental en la comprensión del cáncer, su tratamiento y su prevención.
En este artículo, exploraremos las diversas aplicaciones de la bioinformática en la investigación del cáncer, enfocándonos en cómo estas técnicas han transformado el diagnóstico, el tratamiento y la investigación en general. Desde la secuenciación de genomas tumorales hasta la identificación de biomarcadores, la bioinformática está revolucionando la forma en que entendemos el cáncer y nos permite personalizar enfoques terapéuticos. Acompáñanos en este recorrido por el fascinante mundo de la bioinformática y su papel central en la lucha contra el cáncer.
- La secuenciación genómica y su importancia en el estudio del cáncer
- Identificación de biomarcadores y su potencial en el diagnóstico precoz
- Integración de datos ómicos: una visión holística del cáncer
- Análisis de datos clínicos: un enfoque basado en evidencia
- Retos y perspectivas futuras en el uso de bioinformática en cáncer
- Conclusión: El futuro de la bioinformática en la investigación del cáncer
La secuenciación genómica y su importancia en el estudio del cáncer
La secuenciación genómica ha cambiado la narrativa de la investigación del cáncer al ofrecer una ventana sin precedentes a las alteraciones genéticas que conducen a la formación y progresión de tumores. Mediante el uso de tecnologías avanzadas como la secuenciación de nueva generación (NGS), los científicos ahora pueden analizar múltiples muestras tumorales simultáneamente. Esto no solo acelera el proceso de investigación, sino que también permite la detección de mutaciones raras que podrían ser pasadas por alto en métodos más tradicionales.
Uno de los avances más significativos en este ámbito es la capacidad de realizar análisis comparativos entre el tejido tumoral y el tejido sano. Este enfoque elucidatorio permite a los investigadores identificar mutaciones específicas que son responsables del crecimiento tumoral. Igualmente, la secuenciación de exomas ha demostrado ser particularmente efectiva para identificar variantes asociadas a diferentes tipos de cáncer, lo que podría ayudar a determinar la predisposición genética de un individuo a desarrollar la enfermedad.
Además, la integración de datos genómicos con análisis clínicos y fenotípicos ha permitido una nueva era en el tratamiento del cáncer. Por ejemplo, el perfilado molecular de tumores a través de la bioinformática permite la identificación de tratamientos personalizados que pueden mejorar la eficacia del tratamiento y reducir los efectos secundarios, adaptando así las terapias a las características genéticas de cada paciente.
Identificación de biomarcadores y su potencial en el diagnóstico precoz
Los biomarcadores son características biológicas que indican la presencia o el estado de una enfermedad, en este caso, el cáncer. La identificación de biomarcadores a través de la bioinformática ha revolucionado la forma en que los médicos pueden diagnosticar y monitorear la progresión del cáncer. Gracias a los avances en análisis de datos, se pueden identificar patrones en la expresión génica y en las vías metabólicas que son característicos de las células cancerosas.
Los biomarcadores pueden ser utilizados no solo para el diagnóstico, sino también para la predicción de la respuesta al tratamiento y la prognosis de la enfermedad. Por ejemplo, el uso de biomarcadores como el HER2 en cáncer de mama ha permitido identificar pacientes que se beneficiarán de terapias específicas, mejorando así las tasas de supervivencia. La bioinformática facilita la validación y estandarización de estos biomarcadores, asegurando que sean aplicables en la práctica clínica.
Además, la búsqueda de nuevos biomarcadores ha sido potenciadda por el análisis de grandes bases de datos de pacientes. Los estudios de asociación de genoma completo (GWAS) son una herramienta clave en este esfuerzo, al permitir correlacionar variaciones genéticas con rasgos fenotípicos observable en la población, lo que podría dar lugar a nuevas e importantes dianas terapéuticas.
Integración de datos ómicos: una visión holística del cáncer
La investigación del cáncer ha evolucionado hacia un enfoque multi-ómico. Esto significa que no solo se estudian los datos genómicos, sino también proteómicos, metabolómicos y transcriptómicos de las células tumorales. La bioinformática juega un papel fundamental en la integración de estos datos múltiples para proporcionar una visión más completa y precisa del cáncer y su microentorno.
La integración de datos de diferentes niveles “ómicos” ayuda a entender mejor cómo las interacciones biológicas dentro del tumor contribuyen a su crecimiento y resistencia a tratamientos. Por ejemplo, una red de interacciones en la que se mapean las proteínas involucradas en las vías de señalización celular puede revelar cómo el crecimiento tumoral es influenciado tanto por factores genéticos como ambientales.
El uso de modelos computacionales y algoritmos avanzados también permite simular y predecir el comportamiento del cáncer en diferentes entornos, lo que es vital para el desarrollo de nuevas terapias más efectivas. Además, la bioinformática se ha utilizado para identificar posibles vías en las que la combinación de tratamientos puede ser más efectiva, contribuyendo así al enfoque de “medicina personalizada” que se está convirtiendo en el estándar en la oncología.
Análisis de datos clínicos: un enfoque basado en evidencia
La bioinformática no se limita solo al análisis de datos obtenidos en laboratorio, sino que también puede ser aplicada en el análisis de datos clínicos. Esto incluye la recopilación y el análisis de información sobre la presentación clínica, el tratamiento y el seguimiento de pacientes oncológicos. La combinación de estos datos puede generar nuevas hipótesis sobre el tratamiento y la evolución del cáncer, así como ayudar a identificar factores de riesgo y mejorar la toma de decisiones clínicas.
El uso de modelos predictivos basados en la bioinformática permite a los médicos estimar el pronóstico de los pacientes al identificar correlaciones entre características clínicas y respuesta al tratamiento. Con el tiempo, esto puede llevar a recomendaciones más precisas sobre el manejo de la enfermedad, en función de los datos subjetivos obtenidos de tratamientos anteriores.
Además, la aplicación de técnicas de aprendizaje automático está siendo cada vez más común en el análisis de datos clínicos. Estos métodos tienen la capacidad de detectar patrones en grandes conjuntos de datos y proporcionar predicciones sobre la progresión de la enfermedad, optimizando el tratamiento y ofreciendo una atención más enfocada y eficaz.
Retos y perspectivas futuras en el uso de bioinformática en cáncer
A pesar de los avances, el campo de la bioinformática en la investigación del cáncer enfrenta varios retos. Uno de los mayores desafíos es la integración de datos de diferentes fuentes y su estandarización. La variabilidad en los métodos de colección y análisis de datos puede dificultar la interpretación y la reproducibilidad de los resultados. Asimismo, la gestión y almacenamiento de grandes volúmenes de datos plantean desafíos en términos de recursos y capacidades computacionales.
Sin embargo, las perspectivas futuras son muy prometedoras. Las colaboraciones interdisciplinares entre biólogos, clínicos e informáticos están dando lugar a avances significativos en la forma en que se investiga el cáncer. La creación de bases de datos accesibles y la estandarización de métodos representarán un paso importante hacia la utilización efectiva de la bioinformática en la práctica clínica.
Además, con el creciente enfoque en la inteligencia artificial y el aprendizaje automático, habrá un potencial ilimitado para descubrir nuevas biomarcadores, comprender mecanismos de enfermedad y desarrollar tratamientos innovadores, lo que aumentará las posibilidades de éxito en la lucha contra el cáncer.
Conclusión: El futuro de la bioinformática en la investigación del cáncer
La bioinformática ha demostrado ser una herramienta invaluable en la investigación del cáncer, abriendo nuevas vías para su diagnóstico y tratamiento. Desde la secuenciación de genomas hasta la identificación de biomarcadores únicos, su impacto es profundo y multifacético. Al integrar datos de diferentes niveles y aplicar el análisis clínico adecuado, los investigadores están en una posición estratégica para desarrollar enfoques más personalizados y efectivos contra esta enfermedad devastadora.
El camino por delante está lleno de desafíos, pero también de oportunidades. La colaboración entre distintas disciplinas y el uso de nuevas tecnologías ofrecerán a la investigación del cáncer herramientas más potentes que nunca. En consecuencia, la bioinformática se convertirá en un pilar esencial en la lucha contra el cáncer, revelando insights que podrían, algún día, transformar la manera en que manejamos y atendemos a los pacientes a nivel global.
Si quieres conocer otros artículos parecidos a Bioinformática: Aplicaciones en la investigación del cáncer puedes visitar la categoría Aplicaciones.



Deja una respuesta