
Bioinformática estructural y su relación con la genómica
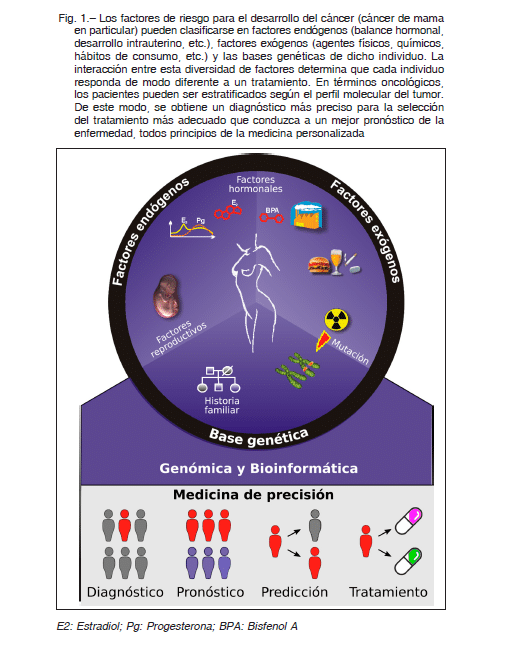
La bioinformática estructural ha emergido como un componente crucial en la investigación biomédica moderna, proporcionando herramientas y enfoques que permiten analizar y modelar la estructura de macromoléculas biológicas. En un mundo donde la información genética está disponible en abundancia, entender cómo se pliegan las proteínas y cómo interactúan con diversas biomoléculas es fundamental para el desarrollo de nuevas terapias y fármacos. Este campo interdisciplinario combina principios de biología, química, informática y matemáticas, creando un puente entre la teoría y la práctica en la exploración de la vida a nivel molecular.
Este artículo se propone explorar en profundidad la sinergia entre la bioinformática estructural y la genómica, dos áreas que, si bien pueden parecer distintas, se entrelazan de maneras fascinantes. A medida que avanzamos, discutiremos cómo la bioinformática estructural contribuye a la interpretación de los datos genómicos y cómo la genómica, a su vez, proporciona insumos valiosos para el modelado y la predicción de estructuras biológicas. A través de diversos ejemplos y estudios de caso, se pondrán de manifiesto las aplicaciones prácticas de esta interrelación en la investigación biomédica y la medicina personalizada.
- Fundamentos de la bioinformática estructural
- La genómica y su papel en la investigación biomédica
- Interrelación entre bioinformática estructural y genómica
- Estrategias computacionales en la bioinformática estructural
- Aplicaciones prácticas en la investigación médica
- Desafíos y futuro de la bioinformática estructural y la genómica
- Conclusión
Fundamentos de la bioinformática estructural
La bioinformática estructural se centra en el estudio y la predicción de las estructuras tridimensionales de biomoléculas, principalmente proteínas y ácidos nucleicos. Una de las herramientas más esenciales en este campo es la cristalografía de rayos X, que permite determinar la disposición atómica de una molécula. Sin embargo, este método puede ser complejo y no siempre es práctico, lo que ha llevado al desarrollo de métodos de modelado computacional, que incluyen el modelado por homología y el simulador de dinámica molecular.
El modelado por homología, por ejemplo, se basa en la idea de que las moléculas similares comparten características estructurales. Los algoritmos de alineación de secuencias pueden identificar regiones conservadas, lo que permite a los investigadores inferir la estructura de una proteína de interés a partir de estructuras que ya han sido determinadas experimentalmente. Este enfoque ahorra tiempo y recursos, facilitando la investigación sobre proteínas para las cuales no se dispone de datos estructurales directos.
La genómica y su papel en la investigación biomédica
La genómica, por su parte, es el estudio del conjunto completo de ADN de un organismo, incluyendo la secuencia de genes y las interacciones entre ellos. Con los avances en tecnologías de secuenciación, se ha podido acceder a información genética a una escala sin precedentes, permitiendo a los científicos estudiar no solo los elementos individuales de la genética, sino también cómo estos se integran para formar sistemas biológicos complejos. Este vasto banco de datos es esencial para identificar variaciones genéticas que puedan estar relacionadas con enfermedades.
A medida que la secuenciación del genoma se vuelve más accesible, la genómica está ayudando a desentrañar la base genética de muchas enfermedades, desde trastornos hereditarios hasta cáncer. Esto se logra mediante el análisis de la variación genética y su relación con el fenotipo o las características observables de un organismo. En este punto, la bioinformática estructural juega un papel crucial al proporcionar modelos estructurales que puedan predecir cómo las mutaciones en el ADN afectan la estructura y función de las proteínas, abriendo nuevas vías para el descubrimiento de fármacos.
Interrelación entre bioinformática estructural y genómica
La interrelación entre la bioinformática estructural y la genómica se manifiesta de diversas maneras en la investigación biomédica. Primero, la estructura de una proteína puede ser influenciada directamente por la secuencia genética que codifica para ella. Cuando se identifican mutaciones en los genes mediante estudios genómicos, es fundamental correlacionar estas alteraciones con cambios estructurales en las proteínas correspondientes. Esto puede permitir la predicción de cómo una mutación específica podría impactar la función biológica, lo que tiene implicaciones directas para la creación de terapias dirigidas.
Por ejemplo, en el caso de ciertas formas de cáncer, los oncogenes pueden haber acumulado mutaciones que alteran la forma en que se pliegan las proteínas. Mediante el uso de bioinformática estructural, los investigadores pueden modelar estas variantes y determinar cómo afectan la interacción de la proteína con su entorno molecular. Esta información es vital para diseñar fármacos que puedan restaurar o modificar la función de las proteínas alteradas en la enfermedad.
Estrategias computacionales en la bioinformática estructural
Las estrategias computacionales implementadas en bioinformática estructural son diversas, desde la predicción de estructuras hasta el análisis de simulaciones moleculares. Por un lado, se utilizan software y herramientas que permiten a los investigadores modelar interacciones proteína-proteína y proteína-ADN, lo que ofrece una visión más clara de las redes de interacción en las que las proteínas están involucradas. Por otro lado, las simulaciones de dinámica molecular permiten observar el movimiento de las moléculas a lo largo del tiempo, proporcionando información valiosa sobre la estabilidad estructural y la función dinámica de las biomoléculas.
Estos enfoques son especialmente útiles en la medicina personalizada, ya que permiten a los investigadores conocer la estructura de las proteínas implicadas en una condición o enfermedad particular y evaluar cómo diferentes tratamientos podrían afectar su comportamiento. La ingeniería de proteínas, otra aplicación clave, utiliza estos métodos para diseñar proteínas con funciones específicas o propiedades mejoradas, lo que puede ser crítico en el desarrollo de nuevos fármacos y terapias biológicas.
Aplicaciones prácticas en la investigación médica
Las aplicaciones de la sinergia entre la bioinformática estructural y la genómica son amplias y variadas. En el desarrollo de nuevos tratamientos, por ejemplo, los investigadores pueden utilizar estos enfoques combinados para diseñar inhibidores específicos para proteínas mutadas en células cancerosas. Este proceso implica identificar dianas moleculares, modelar la estructura de las proteínas afectadas y predecir cómo los posibles fármacos se unirían a estas proteínas.
Además, se puede utilizar la bioinformática estructural para investigar trastornos hereditarios. Al estudiar las variaciones genéticas en familias afectadas por una enfermedad genética, es posible identificar mutaciones que impactan la estructura y función de proteínas críticas. Con esta información, se pueden establecer programas de cribado para identificar individuos en riesgo, así como desarrollar estrategias de tratamiento que aborden el problema a nivel molecular.
Desafíos y futuro de la bioinformática estructural y la genómica
A pesar de los avances significativos, todavía existen desafíos en la interrelación entre la bioinformática estructural y la genómica. Uno de los principales obstáculos es la interpretación de grandes cantidades de datos genómicos. Aunque se cuenta con herramientas computacionales avanzadas, la extracción de información relevante y su colaboración con modelos estructurales sigue siendo un reto. Además, los datos a menudo provienen de diferentes fuentes y pueden ser inconsistentes, lo que dificulta su integración.
Sin embargo, el futuro parece prometedor. Se espera que las innovaciones en machine learning y inteligencia artificial mejoren la capacidad de interpretar datos complejos y refuercen las herramientas de predicción estructural. Esto permitirá, en última instancia, una mejor comprensión de las consecuencias biológicas de las mutaciones genéticas, facilitará el descubrimiento de nuevos fármacos y revolucionará la medicina personalizada.
Conclusión
La bioinformática estructural y la genómica han encontrado un terreno común que promete transformar la investigación biomédica. La capacidad de combinar la vasta información de la genómica con modelos estructurales de proteínas permite una visión más profunda de las bases moleculares de las enfermedades. A medida que avanzamos en la integración de estas disciplinas, se abren nuevas posibilidades para el desarrollo de tratamientos más efectivos y la implementación de la medicina personalizada. En este contexto, el futuro de la investigación médica depende en gran medida de la continua evolución de estas herramientas y enfoques, que seguirán desempeñando un papel central en la comprensión y el tratamiento de enfermedades en las próximas décadas.
Si quieres conocer otros artículos parecidos a Bioinformática estructural y su relación con la genómica puedes visitar la categoría Genómica.



Deja una respuesta