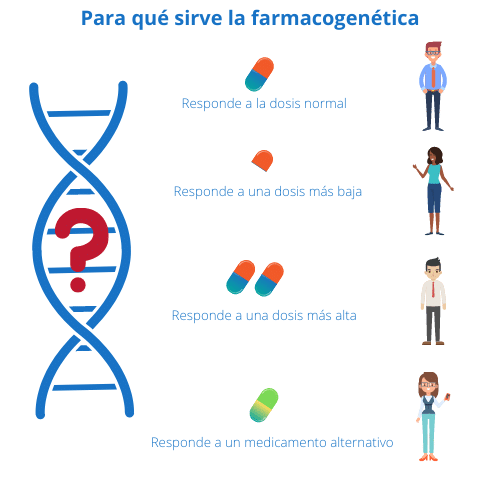
Cómo se estudian las variantes raras en farmacogenómica
La farmacogenómica es una disciplina fascinante que combina la farmacología y la genómica para entender cómo las diferencias genéticas entre individuos afectan su respuesta a medicamentos. En un mundo donde el tratamiento personalizado está ganando impulso, las variantes raras en el ADN juegan un papel crucial, ya que pueden afectar la eficacia y la seguridad de los fármacos. Asimismo, el estudio de estas variantes se convierte en un elemento esencial para mejorar la terapia médica, logrando así una atención más precisa y efectiva para cada paciente.
Este artículo se adentra en el complejo y especializado mundo de las variantes raras en la farmacogenómica, explorando los métodos y técnicas utilizados para su identificación y análisis. A través de diferentes secciones, abordaremos cómo estas variantes se relacionan con la respuesta individual a los medicamentos, los retos asociados a su estudio y las futuras direcciones de la investigación en este campo. El conocimiento claro y preciso sobre estas variantes no solo incrementa nuestra comprensión de la medicación en general, sino que también respalda el desarrollo de terapias más seguras y efectivas.
Entendiendo las variantes raras en el contexto farmacogenómico
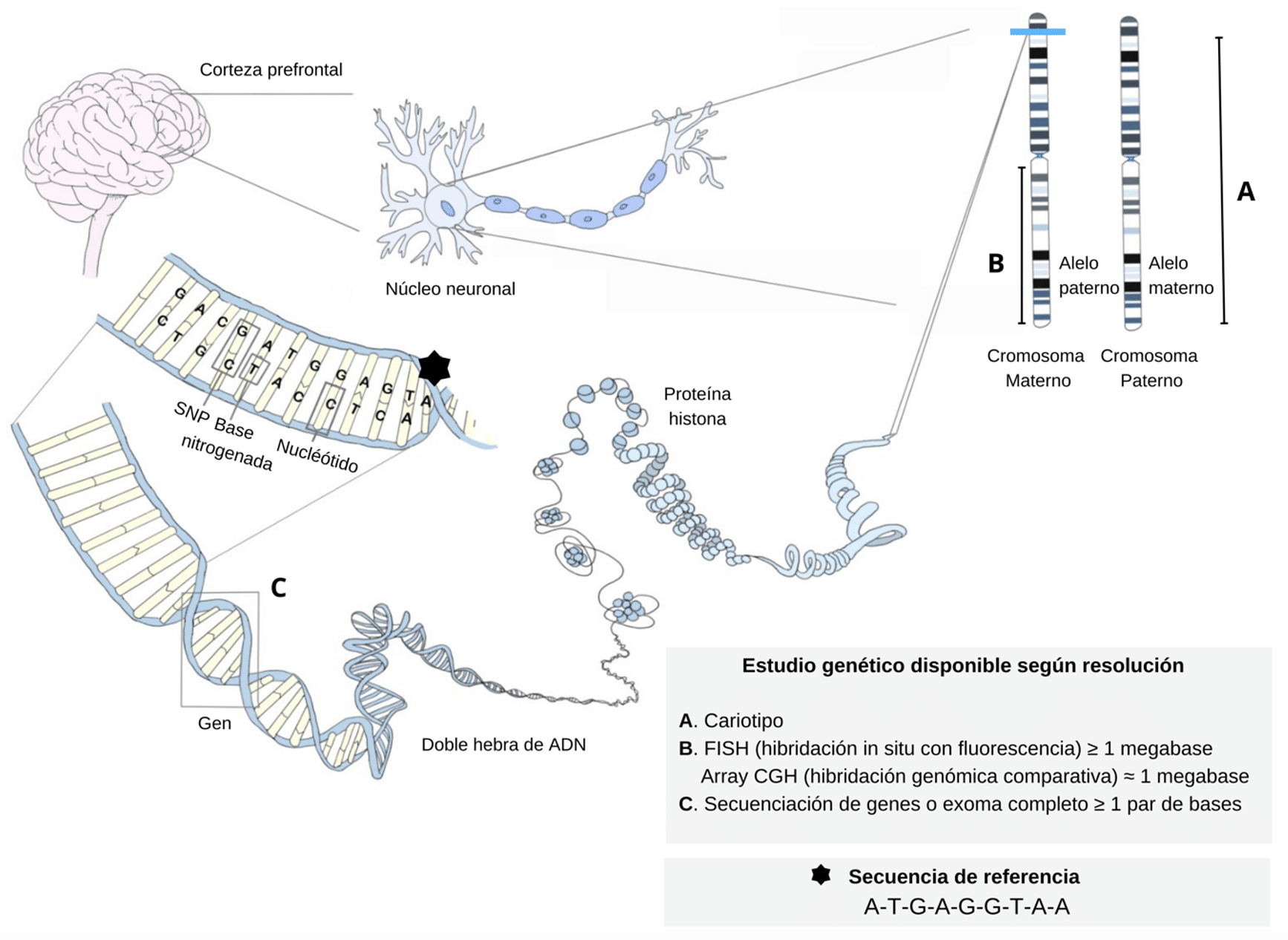
Las variantes raras son alteraciones en el ADN que se encuentran en menos del 1% de la población. Estas variaciones pueden ser desde un solo nucléotido --conocidas como SNP (polimorfismos de nucleótido único)-- hasta más grandes deleciones o inserciones de secuencias genéticas. En el contexto de la farmacogenómica, las variantes raras tienen un papel significativo, ya que pueden influir en cómo un individuo metaboliza un medicamento, su sensibilidad a efectos adversos o incluso su propensión a desarrollar una determinada enfermedad.
Por ejemplo, un paciente con una variante rara en un gen que codifica una enzima metabólica podría no metabolizar adecuadamente un medicamento, resultando en niveles terapéuticos subóptimos o potencialmente tóxicos. Esto hace que la identificación y el estudio de estas variantes sean cruciales para lograr una medicina personalizada. La farmacogenómica busca comprender esos mecanismos para poder adaptar los tratamientos a la variabilidad genética de los pacientes, haciendo el proceso de tratamiento mucho más seguro y efectivo.
Métodos para estudiar variantes raras en farmacogenómica
El estudio de las variantes raras entra en el ámbito de varias metodologías avanzadas de análisis genético. Entre estas, destacamos dos enfoques fundamentales: el **secuenciación de nueva generación** (NGS) y el **análisis de asociación de genoma completo** (GWAS). La secuenciación de nueva generación ha revolucionado el campo de la genómica, permitiendo la secuenciación de múltiples genes de manera rápida y a un costo relativamente bajo. Esto hace posible la identificación de variantes raras en un contexto clínico.
Por otro lado, el análisis de asociación de genoma completo, aunque tradicionalmente se ha utilizado para identificar variantes comunes asociadas con enfermedades, también puede proporcionar información valiosa sobre variantes raras. Ambos enfoques requieren algoritmos bioinformáticos sofisticados para analizar y filtrar grandes volúmenes de datos genómicos, con el objetivo de identificar aquellas variantes que podrían tener impacto en la farmacología. Este análisis no solo busca correlaciones entre variantes y respuesta a tratamientos, sino que también tiene en cuenta factores como el entorno y otros aspectos clínicos del paciente.
Desafíos en el estudio de variantes raras
A pesar de los avances tecnológicos, el estudio de las variantes raras en farmacogenómica presenta muchos retos. Uno de los principales obstáculos es la baja frecuencia de estas variantes en la población, lo que dificulta su detección y análisis. Además, la interpretación de los efectos funcionales de las variantes genéticas raras es a menudo complicada, ya que falta información sobre cómo estas variantes influyen en el metabolismo de fármacos o en la manifestación de enfermedades.
Otro desafío importante es la heterogeneidad genética entre diferentes poblaciones. Esto significa que una variante considerada como "rara" en una población puede ser más común en otra, complicando aún más la búsqueda de relaciones entre variantes y respuesta a medicamentos. Asimismo, la ausencia de datos clínicos a largo plazo sobre los efectos de estas variantes en la población y sus interacciones con diversos medicamentos hace necesario el establecimiento de bases de datos genómicos exhaustivos que proporcionen contexto y referencias válidas para su estudio.
Importancia de la validación clínica
Una vez que se han identificado y caracterizado las variantes raras, la validación clínica es fundamental para confirmar su relación con la respuesta a tratamientos específicos. Este proceso puede incluir ensayos clínicos y estudios poblacionales para evaluar cómo las variantes afectan la eficacia y la seguridad de un medicamento en la práctica clínica real. La integración de la farmacogenómica en la práctica médica viene con la responsabilidad de garantizar que los descubrimientos científicos se traduzcan de manera efectiva en mejoras en la atención al paciente.
La validación clínica también tiene implicaciones éticas y sociales, ya que puede influir en la toma de decisiones médicas y en la relación entre médicos y pacientes. Es esencial que los médicos estén bien informados sobre cómo las variantes raras pueden impactar sus tratamientos y que se establezcan protocolos para compartir esta información con los pacientes de manera clara y comprensible.
El futuro de la farmacogenómica y variantes raras
La farmacogenómica está en constante evolución, y se prevé que las variantes raras continúen siendo un área de crecimiento e interés en el futuro. La disminución de los costos de secuenciación, junto con el desarrollo de algoritmos potentes de análisis computacional y herramientas bioinformáticas sofisticadas, están abriendo nuevas posibilidades para la identificación y análisis de estas variantes. Además, a medida que se acumulan más datos genéticos y clínicos en bases de datos, la posibilidad de correlacionar variantes raras con respuestas a medicamentos y efectos adversos se vuelve más realista.
El impulso hacia una atención médica más personalizada impulsará el desarrollo de estrategias terapéuticas que consideren las variantes raras de manera integral, permitiendo una atención más ajustada a las características individuales de cada paciente. Este camino no solo se trata de tratamientos más eficaces, sino también de prevenir efectos adversos y optimizar el uso de recursos en el manejo de la salud
La investigación en farmacogenómica es crucial para construir un futuro donde todos los pacientes reciban la mejor atención posible basada en su perfil genético, y donde las variantes raras sean entendidas y abordadas como un elemento clave en el desarrollo y uso de fármacos.
Conclusión
El estudio de las variantes raras en farmacogenómica es un campo en constante crecimiento que ofrece la promesa de tratamientos más precisos y eficaces. Desde la identificación de variantes mediante tecnología avanzada como la secuenciación de nueva generación, hasta la validación clínica para garantizar su apropiado uso en la práctica médica, cada paso en este proceso es fundamental. A medida que la ciencia avanza y se superan los retos asociados con estas variantes, será posible integrar en la atención médica los hallazgos sobre la genética del paciente y su impacto en la farmacología. Con una visión hacia el futuro, podemos anticipar un mundo de atención médica más individualizada, promoviendo así una salud general mejor y una calidad de vida óptima para todos.
Si quieres conocer otros artículos parecidos a Cómo se estudian las variantes raras en farmacogenómica puedes visitar la categoría Farmacogenómica.




Deja una respuesta