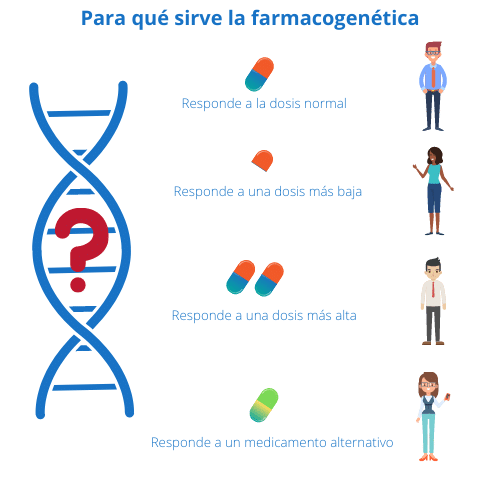
SNPs en farmacogenómica: Implicaciones en tratamientos personalizados
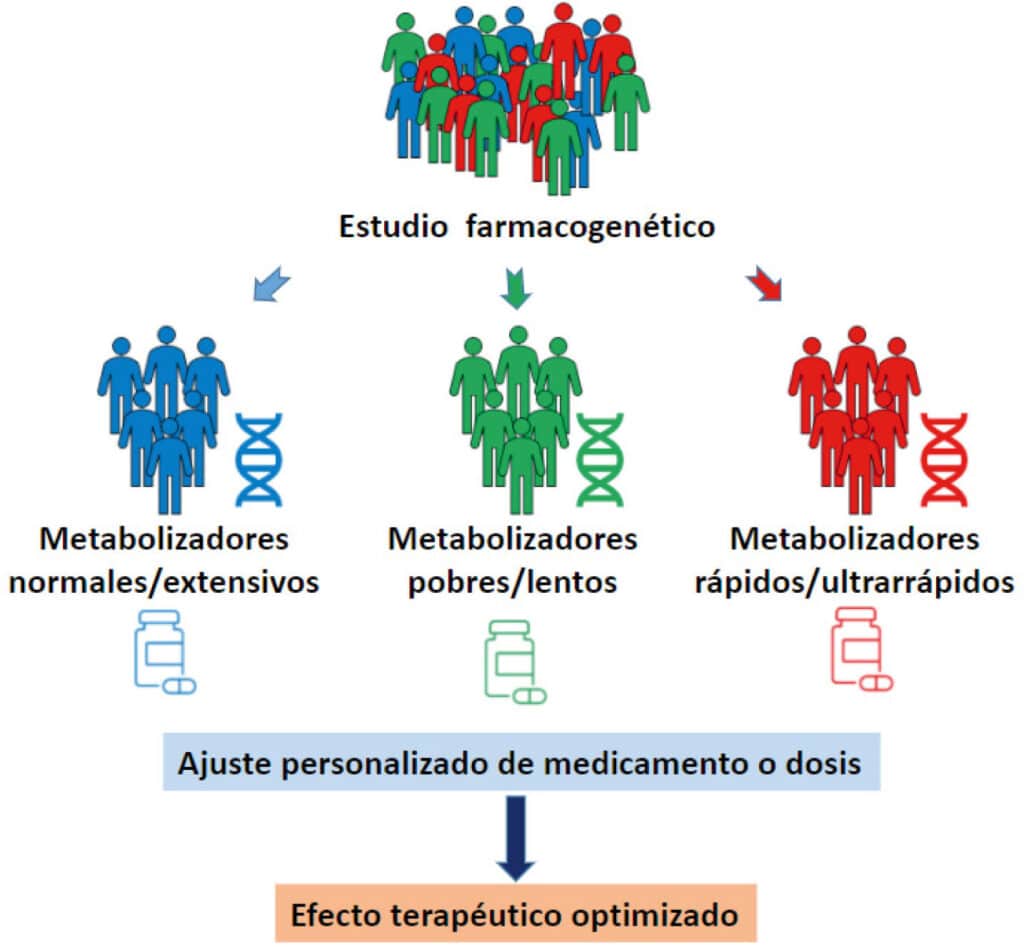
La farmacogenómica es una ciencia que combina la farmacología con la genética, permitiendo comprender cómo las variaciones en el ADN influyen en la respuesta individual a los medicamentos. En este contexto, los SNPs (polimorfismos de un solo nucleótido) emergen como elementos clave que pueden determinar la eficacia y seguridad de los tratamientos en cada paciente. Esta conexión entre genética y medicina ha llevado a un nuevo paradigma en el diseño de terapias personalizadas, lo que promete un futuro donde el tratamiento puede ser optimizado de acuerdo con la constitución genética de cada individuo.
En el presente artículo, exploraremos en profundidad los SNPs y su relevancia dentro de la farmacogenómica. Discutiremos cómo estas pequeñas variaciones en la secuencia del ADN pueden influir en la respuesta a diferentes fármacos, así como sus implicaciones para el desarrollo de tratamientos personalizados. A medida que avanzamos, también abordaremos los retos y oportunidades que se presentan en esta fascinante área de la medicina, buscando conectar ciencia y práctica clínica para mejorar la calidad de vida de los pacientes.
¿Qué son los SNPs?
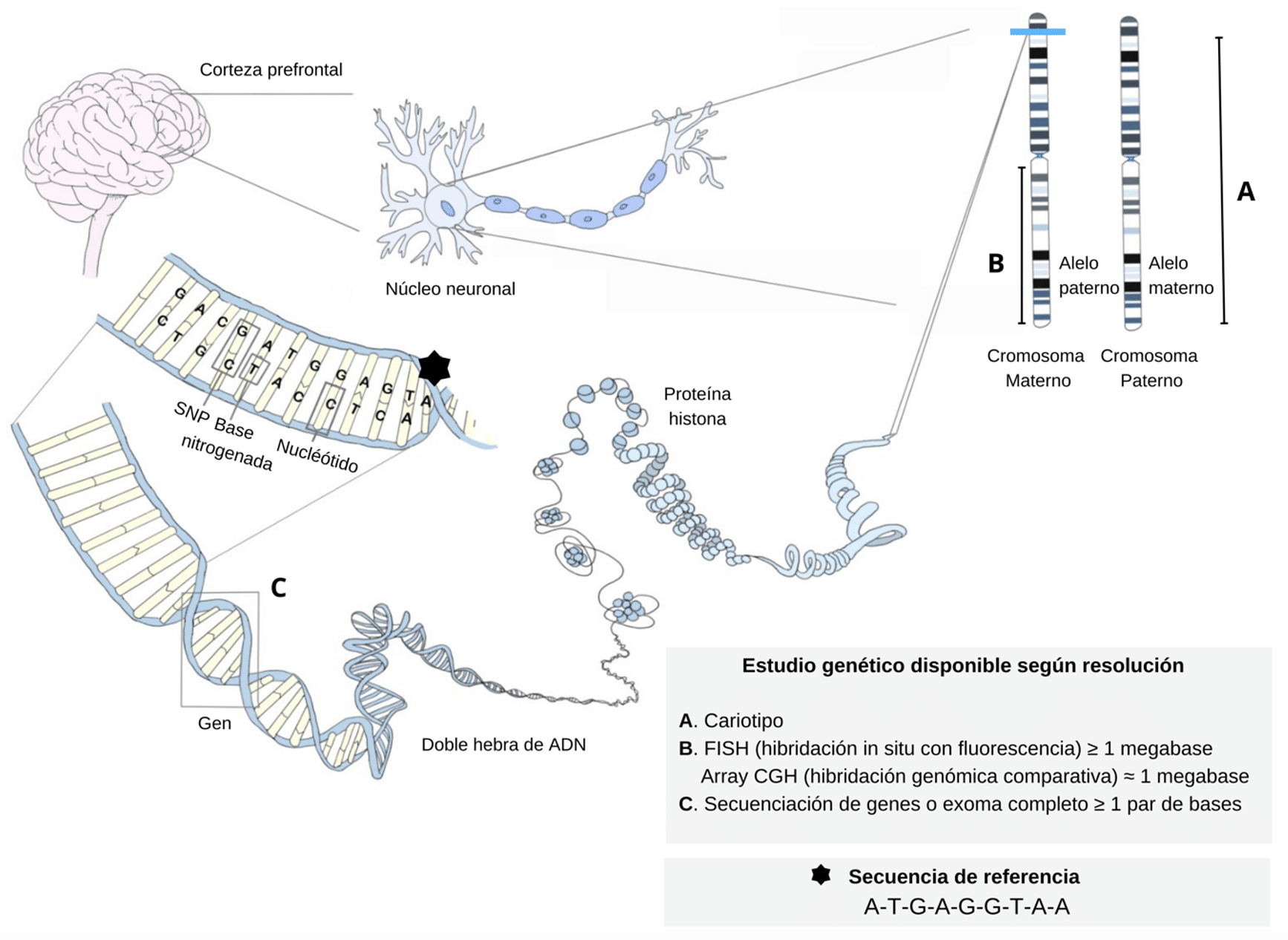
Los SNPs o polimorfismos de un solo nucleótido son variaciones en una sola unidad básica de la secuencia del ADN. Cada SNP representa una diferencia en una sola letra en la secuencia del código genético. Por ejemplo, en un caso de un SNP, un nucleótido adenosina (A) puede ser reemplazado por un nucleótido timina (T). Este tipo de variaciones puede ocurrir en los genes o en regiones del ADN que no codifican proteínas. Aunque la mayoría de los SNPs no tienen un efecto directo en la salud o el desarrollo de enfermedades, algunos pueden influir en cómo las personas responden a medicamentos, lo que los convierte en un foco de estudio crucial en la farmacogenómica.
Los SNPs se encuentran distribuidos a lo largo del genoma humano, con millones de ellos presentes. En general, estos SNPs pueden ser clasificados como sinónimos, donde la variación no afecta la proteína resultante, o no sinónimos, donde la variación cambia la secuencia de aminoácidos de una proteína. Esta clasificación es fundamental para entender cómo un SNP puede influir en la respuesta a un fármaco, ya que algunos pueden alterar la función de proteínas esencialmente involucradas en el proceso de metabolización de los medicamentos.
El papel de los SNPs en la farmacogenómica
La farmacogenómica estudia cómo las variaciones genéticas, especialmente los SNPs, afectan la respuesta de un paciente a los medicamentos. Esta disciplina tiene como objetivo personalizar el tratamiento médico basándose en el perfil genético de cada individuo, lo que puede resultar en regímenes de medicamentos más eficaces y con menos efectos adversos. Por ejemplo, ciertos SNPs pueden influir en la forma en que un fármaco se metaboliza en el hígado o en su interacción con receptores celulares, lo que a su vez puede alterar su eficacia.
Un claro ejemplo de la importancia de los SNPs en farmacogenómica se observa en el caso de medicamentos utilizados para tratar el cáncer. Algunos tratamientos quimioterapéuticos son metabolizados de manera diferente por dos personas debido a la presencia de SNPs en los genes que codifican las enzimas responsables de esta metabolización. Tal diferencia puede determinar si un medicamento será eficaz o, si por el contrario, producirá efectos secundarios graves. Por esta razón, la evaluación de los SNPs previos a la terapia se está volviendo cada vez más común en la práctica clínica, buscando mejorar la predicción de la eficacia del tratamiento y minimizar los riesgos.
Implicaciones clínicas de los SNPs en el tratamiento de enfermedades
La aplicación de la farmacogenómica en la medicina personalizada implica múltiples implicaciones clínicas. Primero, el descubrimiento de SNPs que afectan a la farmacocinética o farmacodinámica de los medicamentos puede llevar a la modificación de dosis para maximizar los beneficios de un tratamiento. En situaciones donde un SNP específico se asocia con una menor producción de una enzima relacionada con la metabolización de un fármaco, se puede optar por ajustar las dosis a la baja para prevenir toxicidades.
Adicionalmente, comprender cómo los SNPs afectan la respuesta a tratamientos permite a los profesionales de la salud elegir entre diferentes opciones terapéuticas. Por ejemplo, en el caso de personas con variaciones en los genes que influyen en la respuesta al metabolismo de anticoagulantes, se puede seleccionar un tipo de medicamento que sea menos susceptible a ser afectado por esas variaciones, asegurando así una mayor seguridad y eficacia. Este enfoque no solo mejora la eficacia del tratamiento, sino que también resulta en una reducción de costes al evitar tratamientos poco efectivos o que producen efectos adversos.
Retos y oportunidades en la implementación de la farmacogenómica
A pesar de las promesas que los SNPs y la farmacogenómica ofrecen, también existen retos que debo ser abordados para garantizar su efectiva integración en la práctica clínica. Uno de los principales desafíos es la normalización de las pruebas genéticas necesarias para identificar variaciones genéticas. La falta de estándares uniformes podría llevar a inconsistencias en los resultados y, por ende, a decisiones clínicas que no estén basadas en datos precisos.
Otro reto importante es la interpretación de los resultados genéticos. Con millones de SNPs posibles, a menudo no está claro cuáles son relevantes para la respuesta a medicamentos específicos. Utilizar algoritmos avanzados y herramientas de inteligencia artificial para interpretar estos datos puede ser una solución, pero también plantea cuestiones sobre el acceso y la equidad en el cuidado de la salud. Además, es esencial garantizar la privacidad y la seguridad de la información genética del paciente.
El futuro de la farmacogenómica y los SNPs
El futuro de la farmacogenómica y el papel de los SNPs en la medicina personalizada es prometedor. Cada vez más, se están realizando estudios genéticos que permiten identificar y validar nuevos SNPs asociados con respuestas a tratamientos, lo que sugiere que la personalización del tratamiento se convertirá en una norma y no en una excepción. Además, la creciente disponibilidad de tecnologías de secuenciación del ADN a bajo coste permite una mayor exploración de la variabilidad genética y su relación con las respuestas a los medicamentos.
Una tendencia que está ganando impulso es la creación de bases de datos que integran información genómica con datos clínicos, lo que podría ofrecer a los investigadores y clínicos una herramienta poderosa para correlacionar SNPs con respuestas a medicamentos en poblaciones diversas. Con el tiempo, esta integración puede conducir a un enfoque más holístico y efectivo en el tratamiento de enfermedades, mejorando no solo la eficacia de los tratamientos, sino también la calidad de vida de los pacientes.
Conclusión
Los SNPs desempeñan un papel fundamental en el ámbito de la farmacogenómica, ofreciendo una ventana hacia la personalización de los tratamientos médicos en función de la genética individual. A lo largo del artículo, hemos examinado cómo estas variaciones genéticas influyen en la eficacia y seguridad de los medicamentos, abriendo paso a prácticas clínicas más informadas y personalizadas. Sin embargo, los desafíos para la implementación efectiva de estas pruebas en la práctica real son significativos, pero no insuperables. A medida que se avanza en la investigación y se integran nuevas tecnologías, es probable que la farmacogenómica se convierta en un pilar esencial en el tratamiento moderno de enfermedades. La conexión entre SNPs y terapias personalizadas no solo redefine la forma en que concebimos los tratamientos, sino que también promete optimizar la atención médica y mejorar radicalmente la experiencia de los pacientes.
Si quieres conocer otros artículos parecidos a SNPs en farmacogenómica: Implicaciones en tratamientos personalizados puedes visitar la categoría Farmacogenómica.




Deja una respuesta